【成果】细胞内囊泡输运的三维时空动力学特征及调控机制
囊泡输运是细胞内物质、能量和信息交换的主要途径,也是细胞多种生理功能实现和调控的物理基础。病毒侵染细胞的过程也依赖于囊泡输运。囊泡输运的异常与发育问题、以及神经退行性和免疫等疾病密切相关。与溶液中不同,细胞内部是一种活性的非平衡系统,造就了细胞内输运行为的复杂性:在扩散方面,区别于布朗运动,表现为在热涨落、活性涨落、结构异质性、拥挤环境共同影响下的异常扩散;在长距离输运方面,马达蛋白通过atp水解释放的能量,可驱动更加有效的定向运输。然而,过去针对细胞内输运的研究主要借助于二维成像技术,一直缺乏对于细胞内真实的三维输运动力学及其调控机制的深入了解。
北京师范大学系统科学学院/非平衡系统研究所的李辉教授长期开展生物复杂系统的动力学研究,通过发展活细胞单分子动态成像技术和定量分析方法,系统研究了细胞内的生物大分子输运动力学:扩散方面,发现了内质网结构导致的细胞内扩散异质性[j. am. chem. soc. 137, 436 (2015)],以及细胞内扩散的准二维特性[cpl express letters 37, 078701 (2020)];定向运输方面,发现了凋亡细胞内的输运加[pnas 115, 12118 (2018)],以及无膜细胞器的定向运输[faseb journal 32, 5891 (2018)]。

近期,李辉教授与中科院物理所王鹏业研究员和杨明成研究员等团队合作,基于前期搭建的三维单颗粒荧光追踪成像平台,研究了细胞内囊泡输运的三维时空动力学特征及调控机制。研究发现,细胞内囊泡输运随着测量时间尺度表现出不同的动力学特征,即在小于0.1s时间内为三维受限运动,大于0.1s时转变为xy方向的准二维运动。在细胞内空间分布方面,囊泡的横向运动(xy方向)表现出明显的空间异质性,细胞外周比细胞核周边的运动更快;而囊泡的轴向运动(z方向)则在整个细胞内较为匀质。
进一步,研究揭示了囊泡输运动力学的细胞骨架调控机制。其中,微丝骨架(actin filament)对囊泡施加了三维各向同性的约束限制,微管骨架(microtubule)则借助马达蛋白驱动囊泡产生xy方向的定向运动,而后者需要一定时间的累积才变得显著。因此,在短时间尺度内,囊泡表现为热涨落驱动和微丝骨架约束共同作用下的三维受限运动;随着时间尺度的增加,囊泡运动在马达蛋白活性驱动和微管骨架空间结构的共同影响下,转变为各向异性和空间异质性的动力学特征。
在囊泡内部,该研究首次发现当微管骨架被解聚后,内吞颗粒能够沿囊泡的内膜扩散,其轨迹呈现出标准的球壳形状。该结果表明微管骨架不仅能够调控囊泡运输,而且可铆钉囊泡内部的“货物”。
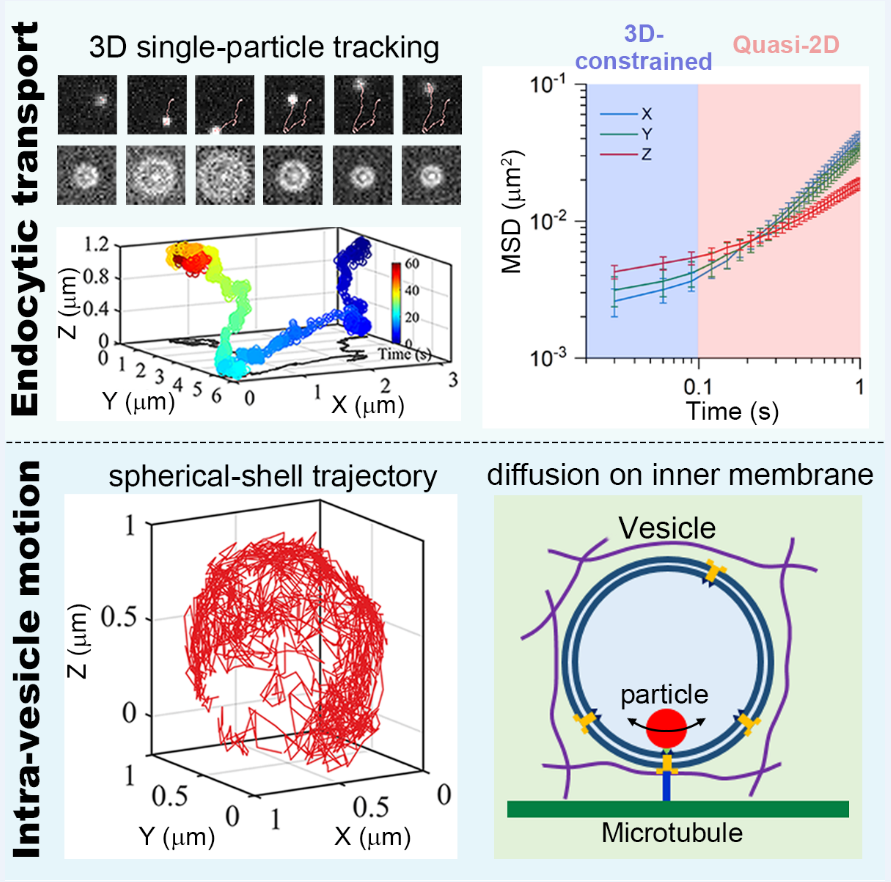
该工作基于三维高时空分辨的单颗粒跟踪技术,揭示了细胞内囊泡三维输运动力学的时空特性,并且阐明了热涨落、活性驱动、及不同细胞骨架对囊泡输运动力学的协同调控机制。该研究有助于深入理解囊泡输运的生物功能,以及病毒在细胞中的转运机制。
该工作以“spatiotemporal three-dimensional transport dynamics of endocytic cargos and their physical regulations in cells”为题发表在cell子刊《交叉科学iscience》上 [iscience 25, 104210 (2022)],链接。论文的通讯作者是北京师范大学李辉教授、中科院物理所王鹏业研究员和杨明成研究员,第一作者是物理所已毕业博士生江超。该工作得到了国家自然科学基金、科技部重点研发计划、中科院青促会的支持。
作者:李辉
审核:王大辉
编辑:郝林青

